
|
Ciência Florestal
Centro de Pesquisas Florestais - CEPEF, Departamento de Ciências Florestais - DCFL, Programa de Pós Graduação em Engenharia Florestal - PPGEF
ISSN: 0103-9954 EISSN: 1980-5098
Vol. 18, Num. 2, 2008, pp. 143-150
|
Ciência Florestal, Vol. 18, No. 2, 2008, pp. 143-150
Germinação De
Sementes E Crescimento Inicial De Plântulas De Tabebuia aurea (Silva
Manso) Benth. & Hook f. ex S. Moore
Seed Germination And Initial
Growth Of Tabebuia
aurea (Silva
Manso) Benth. & Hook f. ex S. Moore Seedlings
Mauro
Vasconcelos Pacheco1, Valderez Pontes Matos2, Ana
Lícia Patriota Feliciano3, Rinaldo Luiz Caraciolo Ferreira4
1Biólogo, MSc., Doutorando em Ciência e Tecnologia de Sementes, Universidade Federal de Pelotas, Campus
Universitário, s/n, Caixa Postal 354, CEP 96010-900, Pelotas (RS). pachecomv@hotmail.com
2Engenheira Agrônoma, Drª. Professora Associada do Departamento de Agronomia, Universidade Federal Rural de
Pernambuco, Rua Dom Manoel de Medeiros, s/n, Dois Irmãos, CEP 52171-900, Recife (PE). vpmatos@ig.com.br
3Engenheira Florestal, Drª. Professora Associada do Departamento de Ciências Florestais, Universidade Federal
Rural de Pernambuco, Rua Dom Manoel de Medeiros, s/n, Dois Irmãos, CEP 52171-900, Recife (PE).
4 Engenheiro Florestal, Dr. Professor Associado do Departamento de Ciências Florestais, Universidade Federal Rural
de Pernambuco, Rua Dom Manoel de Medeiros, s/n, Dois Irmãos, CEP 52171-900, Recife (PE). Bolsista do CNPq.
rinaldof@ufrpe.br
Recebido para publicação em 5/12/2006 e aceito em 15/04/2008.
Code Number: cf08013
RESUMO
A Tabebuia
aurea (craibeira) é uma espécie arbórea nativa que pode ser utilizada na
recomposição de áreas degradadas, como planta ornamental e fornecedora de madeira
de boa qualidade. O presente trabalho teve como objetivos avaliar o efeito de
diferentes temperaturas e substratos sobre a germinação das sementes e o
crescimento inicial de plântulas de Tabebuia aurea. O delineamento
experimental foi inteiramente casualizado em arranjo fatorial 5 x 5 (cinco
substratos: papel toalha, areia, vermiculita, pó de coco e Tropstrato®; cinco
temperaturas: 25, 30, 35, 20-30 e 20-35ºC), com quatro repetições de 25
sementes cada. Foram avaliados os seguintes parâmetros: germinação, primeira
contagem da germinação, índice de velocidade de germinação, tempo médio de
germinação, comprimento e massa seca da parte aérea e do sistema radicial. As
temperaturas e substratos influenciaram as características avaliadas, exceto a
avaliação final da germinação, a qual variou entre 84 e 94%. As temperaturas
ótimas de germinação foram 30 e 35ºC. Os substratos papel toalha e entre areia
foram mais adequados para avaliação segura da qualidade fisiológica de sementes
de Tabebuia aurea.
Palavras-chave:sementes florestais; temperatura; substrato; vigor.
ABSTRACT
Tabebuia
aurea
is a native arboreal species that can be used in recomposition programs of
degradated areas, as ornamental plant and for production of wood of quality.The objectives of this
study were to evaluate the effects of the temperature and substrate on seed
germination and initial growth of T. aurea seedlings. The experiment was
developed in a completely randomized design in factorial scheme 5 x 5 with
temperatures of 25, 30, 35, 20-30 and 20-35ºC; and substrates: paper towels,
and into sand, vermiculite, coconut fiber and Tropstrato®, with four
replications of 25 seeds each. The following parameters were also analyzed:
germination, first germination count, germination speed index, average time of
germination, length and dry weight matter of the shoot and the root. The
temperatures and substrates influenced the analyzed parameters, except for the
final percentage of germination, which varied from 84 to 94%. The optimal
temperatures for germination were 30 and 35ºC. The substrates paper towels roll
and sand can be recommended to evaluate the physiological quality of T.aurea
seeds.
Keywords:forest seeds;
temperature; substrate; vigor.
INTRODUÇÃO
A
craibeira (Tabebuia aurea (Silva Manso) Benth. & Hook. f. ex. S.
Moore) é uma espécie arbórea, da família Bignoniaceae, com características
morfológicas e ecofisiológicas bastante distintas entre indivíduos encontrados
nos Cerrados e em várzeas úmidas da Caatinga e do Pantanal (LORENZI, 1998). Suas
flores amarelas são extremamente ornamentais, sendo considerada a flor-símbolo
do estado de Alagoas (CARVALHO, 2003). É muito utilizada na arborização urbana
e sua madeira pode ser empregada na construção civil e confecção de móveis
(LORENZI, 1998).
A propagação sexuada de Tabebuia aurea mostra a
necessidade de se desenvolverem estudos sobre a germinação de suas sementes,
uma vez que fatores ambientais, como a temperatura e substrato, são necessários
para desencadear o complexo processo metabólico da germinação (POPINIGIS,
1985).
A temperatura influencia diretamente a
velocidade na qual as reservas nutricionais das sementes são mobilizadas e a
síntese das substâncias necessárias para o desenvolvimento da plântula (BEWLEY
e BLACK, 1994). Portanto, afeta o processo germinativo de três maneiras
distintas, sobre a porcentagem, velocidade e uniformidade de germinação
(CARVALHO e NAKAGAWA, 2000). A germinação ocorre sob limites relativamente
amplos de temperatura cujos extremos dependem, dentre outros fatores,
especialmente da espécie e suas características genéticas (MARCOS FILHO, 2005).
Cada espécie apresenta temperatura ótima para germinação de suas sementes, para
proporcionar a porcentagem máxima de germinação no menor tempo (POPINIGIS,
1985). Existe consenso entre os pesquisadores de que a temperatura para a
germinação não apresenta um valor específico, mas pode ser expressa em termos
das temperaturas cardeais, isto é, mínima, máxima e ótima (MACHADO et al.,
2002).
O efeito da temperatura sobre a germinação de
sementes de Cecropia hololeuca Miq. foi estudado por Godoi e Takaki
(2004), e os resultados obtidos reforçaram a observação na qual a faixa de 20 a 30ºC mostrou-se adequada para a germinação de grande número de sementes de espécies arbóreas
tropicais e subtropicais (BORGES e RENA, 1993). A germinação das sementes de Casearia
sylvestris Sw. e de Psychotria leiocarpa Cham. & Schltdl.
ocorreu, apenas, em temperaturas constantes de 20 e 25ºC (ROSA e FERREIRA,
2001), enquanto que a faixa ótima de temperatura para germinação de sementes de
ipê-amarelo (Tabebuia serratifolia (Vahl) Nicholson) é de 25 a 35ºC (MACHADO et al., 2002).
A distribuição geográfica e ecológica das
espécies pode determinar os limites de temperatura para a germinação das
espécies (ROBERT, 1992). Assim, algumas espécies requerem alternância de
temperatura, esse comportamento geralmente está associado a espécies que
apresentam dormência, mas a alternância também pode beneficiar outras cujas
sementes não apresentam nenhum mecanismo de dormência (MARCOS FILHO, 2005).
A função do substrato é proporcionar à semente condições ambientais
adequadas para a germinação e desenvolvimento inicial da plântula. Assim,
deve-se levar em consideração o tamanho da semente, a exigência com relação à
umidade e à luz, a facilidade que o substrato oferece ao desenvolvimento da
plântula e à avaliação durante as contagens. O substrato também deve ser
atóxico às plântulas, livre de microrganismos, além de apresentar boa aeração e
capacidade de absorção e retenção de água (POPINIGIS, 1985; FIGLIOLIA et al.,
1993).
As Regras para Análise de Sementes recomendam utilizar substratos como
papel, areia e solo para condução de testes de germinação (BRASIL, 1992).
Entretanto, existem poucas recomendações para as espécies florestais nativas e
outros substratos, como a vermiculita, vêm sendo testados com sucesso
(FIGLIOLIA et al., 1993; ANDRADE
et al., 1999; SILVA et
al., 2002).
Além do teste de germinação, devem-se
realizar testes de vigor, pois ambos se complementam para avaliar a qualidade
fisiológica de lotes de sementes (MARCOS FILHO, 1999).
A identificação de diferenças importantes
no potencial fisiológico das sementes, em especial daquelas que apresentam
comportamento semelhante nos testes de germinação, representa o objetivo básico
dos testes de vigor. A eficiência dos testes de vigor depende da escolha
adequada do método em função dos objetivos pretendidos, pois o uso de apenas um
teste pode gerar informações incompletas. Portanto, devem-se combinar
resultados de diferentes testes, tendo em vista a finalidade do uso dos
resultados para se avaliar, com segurança, o potencial fisiológico de um lote
de sementes (MARCOS FILHO, 1999).
O presente estudo teve como objetivos avaliar a
germinação das sementes e o crescimento inicial de plântulas de Tabebuia
aurea em diferentes temperaturas e substratos.
MATERIAL E
MÉTODOS
As
sementes de craibeira foram coletadas em vinte árvores na região metropolitana
de Recife, Pernambuco, em março de 2004. Os experimentos foram conduzidos nos
Laboratórios de Sementes do Departamento de Agronomia e de Sementes Florestais
do Departamento de Ciência Florestal da Universidade Federal Rural de
Pernambuco. O beneficiamento das sementes consistiu na remoção das asas, com o
auxílio de tesouras, e na eliminação de sementes chochas e imaturas e, em
seguida, foram homogeneizadas, acondicionadas em sacos de papel kraft e
armazenadas durante dois meses em câmara fria (16,5ºC e 50% U.R.) (BARBOSA,
2004). As sementes apresentavam teor de água de 9% por ocasião da instalação do
experimento.
Os testes de germinação foram conduzidos em germinadores tipo Biochemical
Oxigen Demand (B.O.D.) às temperaturas de 25, 30, 35, 20-30 e 20-35ºC e
fotoperíodo de 8 horas. Para as temperaturas alternadas, o período luminoso
correspondeu à temperatura mais alta.
As sementes de craibeira foram desinfestadas com solução de hipoclorito
de sódio a 5%, durante 5 minutos e lavadas com água destilada. A semeadura foi
feita entre os substratos papel toalha, areia (BRASIL, 1992), vermiculita
média, pó de coco fino e Tropstrato® autoclavados a 120ºC, durante duas horas,
e umedecidos com solução de Nistatina a 0,2%. Para os quatro últimos
substratos, a semeadura foi feita em caixas acrílicas transparentes de 11 x 11
x 3cm, com tampa. O substrato papel toalha, após semeadura, foi organizado em
forma de rolos (BRASIL, 1992).
O número de sementes germinadas foi avaliado diariamente, adotando-se
como critério de germinação a emergência dos cotilédones, com o conseqüente
surgimento do hipocótilo.
Foram avaliados os seguintes parâmetros: germinação – porcentagem de
sementes germinadas até o final do experimento, 14 dias após a semeadura; primeira
contagem – porcentagem de sementes germinadas até o 5º dia após o início do
teste; índice de velocidade de germinação (IVG) – determinado de acordo
com a fórmula apresentada por Maguire (1962); tempo médio de germinação
(TMG) – de acordo com a fórmula citada por Silva e Nakagawa (1995), com o
resultado expresso em dias após a semeadura; comprimento da parte aérea e da
raiz primária – a parte aérea e a raiz primária das plântulas normais de
cada repetição foram medidas com o auxílio de uma régua graduada em milímetros
e os resultados expressos em cm/plântula; massa seca da parte aérea e do
sistema radicial – as plântulas normais de cada repetição, após a retirada
dos cotilédones, foram acondicionadas em sacos de papel, previamente
identificadas, e levadas à estufa de ventilação forçada, regulada a 80ºC,
durante 24 horas. Após esse período, as plântulas foram retiradas da estufa e
pesadas em balança analítica, com precisão de 0,001 g, sendo os resultados expressos em mg/plântula (NAKAGAWA, 1999).
Foi utilizado o delineamento experimental inteiramente casualizado, com
os tratamentos distribuídos em arranjo fatorial 5 x 5 (cinco temperaturas e
cinco substratos), com quatro repetições de 25 sementes cada. Os dados foram
analisados com o software estatístico SAS System for Windows (Statistical
Analysis System), versão 8.02. SAS Institute Inc, 1999-2001, Cary, NC, USA. As
médias foram comparadas pelo teste de Tukey a 5% de probabilidade. Os dados da
primeira contagem da germinação foram transformados em arc sen 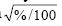 por não atenderem
aos requisitos de homogeneidade de variância e normalidade. por não atenderem
aos requisitos de homogeneidade de variância e normalidade.
RESULTADOS
E DISCUSSÃO
Os resultados de germinação das sementes de craibeira, no 14º dia após
a semeadura, mostraram que não houve efeito (P>0,05) dos substratos e
regimes de temperatura (Tabela 1).
A ampla faixa de temperatura de germinação de sementes de craibeira
apresenta caráter estratégico e adaptativo. Isso permite alta capacidade de
estabelecimento das plântulas em campo, aumentando as chances de sobrevivência
(TOWNSEND e MACGINNIES, 1972). Resultados semelhantes foram obtidos em sementes
de Tabebuia aurea,com temperaturas entre 20 e 40ºC e valores médios de germinação acima de
80% (CABRAL et al., 2003). A faixa de temperatura entre 20 e 30ºC também
foi considerada ótima às sementes de Tabebuia serratifolia (Vahl) G. Nicholson, Tabebuia chrysotricha (Mart. ex A. DC.) Slandl. e Tabebuia roseo-alba (Cham.) Sandwith (SANTOS et al., 2005), bem
como para as sementes de Eremanthus erythropappus (DC.) MacLeish
(TONETTI et al., 2006), pois proporcionou melhor desempenho germinativo
para as sementes dessas espécies.
A primeira contagem da germinação no 5º dia após a instalação do
experimento mostrou interação significativa (P<0,05) entre substratos e
temperaturas com o papel proporcionando melhor desempenho germinativo das
sementes de Tabebuia aurea em todas as temperaturas. O substrato areia, apenas
nas temperaturas constantes de 30 e 35ºC mostrou maiores porcentagens de
germinação na primeira contagem (Tabela 1). Essas temperaturas proporcionaram
comportamento semelhante ao da germinação inicial de sementes de Ocotea
corymbosa (Meissn.) Mez, com melhores valores naquela mais elevada (30ºC),
embora na avaliação final, todas as temperaturas tenham revelado comportamento
semelhante na porcentagem de germinação (BILIA et al.,1998).
TABELA 1: Germinação (%) e primeira
contagem da germinação (%) de sementes de Tabebuia aurea (Silva Manso)
Benth. & Hook. f. ex. S. Moore, submetidas a diferentes temperaturas e
substratos.
TABLE
1: Germination (%) and first germination count (%) of Tabebuia aurea
(Silva Manso) Benth. & Hook. f. ex. S. Moore seeds submitted at different
temperatures and substrates.
|
Substratos |
Temperatura (oC) |
|
25 |
30 |
35 |
20-30 |
20-35 |
|
|
Germinação (%) |
|
Papel |
84 |
90 |
88 |
87 |
86 |
|
Areia |
94 |
93 |
92 |
84 |
91 |
|
Vermiculita |
92 |
89 |
90 |
87 |
86 |
|
Pó
de coco |
94 |
90 |
86 |
88 |
89 |
|
Tropstrato® |
91 |
86 |
90 |
87 |
94 |
|
|
Primeira contagem da germinação (%) |
|
Papel |
83 Aa |
86 Aa |
85 Aa |
86 Aa |
83 Aa |
|
Areia |
11 Bbc |
72 Aa |
60 Aa |
25 Bb |
4 Cc |
|
Vermiculita |
22 Bb |
47 Ba |
22 Bb |
19 BCb |
17 Bb |
|
Pó de coco |
2 Cb |
40 Ba |
33 Ba |
3 Db |
1 Cb |
|
Tropstrato® |
3 Cb |
36 Ba |
36 Ba |
8 CDb |
2 Cb |
Em
que: Médias seguidas pela mesma letra, maiúscula na coluna e minúscula na
linha, não diferem entre si pelo teste de Tukey a 5% de probabilidade.
No substrato areia, a melhor combinação para
a velocidade de germinação foi obtida quando as sementes foram
submetidas a 30 e 35ºC (Tabela 2). Sementes de Schizolobium amazonicum
Huber ex Ducke também tiveram a velocidade de germinação favorecida pelas
temperaturas de 30 e 35ºC em papel toalha, com valores médios de 4,0 e 3,8
respectivamente (RAMOS et al., 2006). Em sementes de Mutingia calabura
L., a temperatura alternada de 20-30ºC favoreceu a velocidade de germinação,
enquanto que a temperatura constante de 30ºC foi responsável pela sua inibição
(LOPES et al., 2002).
O tempo médio de germinação é importante para se avaliar a rapidez de
ocupação de uma espécie em uma comunidade (FERREIRA et al., 2001). Os
menores tempos médios de germinação (Tabela 2) foram alcançados com o substrato
papel em todas as temperaturas. Além disso, a 30ºC foram observados os menores
valores de tempo médio para todos os substratos testados. Sementes de Tibouchina
pulchra (Cham.) Cogn e de Tibouchina sellowiana Cogn. apresentaram
valores semelhantes de aumento na velocidade de germinação e tendência de
redução no tempo médio de germinação (FREITAS, 1998).
As melhores combinações de temperatura e substrato (P<0,05) para o
comprimento da parte aérea das plântulas de craibeira foram proporcionadas pela
temperatura de 35ºC em todos os substratos, exceto entre vermiculita (Tabela
3). Isso pode ser atribuído ao maior incremento da parte aérea, pelo
desenvolvimento do epicótilo, pois com a elevação da temperatura, a velocidade
das reações bioquímicas também aumenta, permitindo o rápido deslocamento das
reservas nutricionais da semente ao eixo embrionário e de substâncias
fotossintetizantes necessárias ao desenvolvimento inicial da parte aérea (CARVALHO
e NAKAGAWA, 2000).
A interação (P<0,05) entre substratos e temperaturas apresentou
maior comprimento médio de raiz no substrato papel toalha a 30ºC (Tabela 3) que
nas temperaturas de 25, 20-30 e 20-35ºC. A maior expressão de vigor em sementes
de Strelitzia reginae Aiton ocorreu quando a semeadura foi feita em
papel toalha a 25ºC, favorecendo o comprimento radicial (BARBOSA et al.,
2005). Esses resultados podem ser atribuídos ao maior espaçamento entre as
sementes de Tabebuia aurea, proporcionado pelo rolo de papel toalha. Além disso,
as variações na temperatura e na umidade do substrato são críticas para o teste
de vigor quando comparadas ao teste de germinação. A diferença de 1ºC na
temperatura, durante o teste de germinação, provavelmente terá efeito
desprezível na porcentagem de germinação, mas essa diferença na temperatura
poderá proporcionar efeitos consideráveis no crescimento das plântulas,
alterando seu comprimento e/ou sua massa seca (NAKAGAWA, 1999).
TABELA 2: Índice de velocidade de germinação
e tempo médio de germinação (dias) de sementes de Tabebuia aurea (Silva
Manso) Benth. & Hook. f. ex. S. Moore, submetidas a diferentes temperaturas
e substratos.
TABLE 2: Index of germination speed and average time
of germination (days) of Tabebuia aurea (Silva Manso) Benth. & Hook.
f. ex. S. Moore seeds submitted at different temperatures and substrates.
|
Substratos |
Temperatura (oC) |
|
25 |
30 |
35 |
20-30 |
20-35 |
|
|
IVG |
|
Papel |
4,17 Aa |
4,41 ABa |
4,30 Aa |
4,32 Aa |
4,23 Aa |
|
Areia |
3,48
Bb |
4,45
Aa |
4,14 ABa |
2,81 Bc |
2,88 Bc |
|
Vermiculita |
3,41
Bab |
3,90
ABCa |
3,42
Cab |
2,60
Bc |
3,04
Bbc |
|
Pó de coco |
3,26 Ba |
3,85 Bca |
3,31 Ca |
2,42 Bb |
2,62 Bb |
|
Tropstrato® |
2,96 Bb |
3,67 Ca |
3,64 BCa |
2,64 Bb |
2,76
Bb |
|
|
TMG (dias) |
|
Papel |
5,1 Ca |
5,2 Aa |
5,3
Ca |
5,0
Ca |
5,1
Ca |
|
Areia |
7,0
Bb |
5,3
Ac |
5,8
BCc |
8,4
Ba |
8,2
ABa |
|
Vermiculita |
7,3
ABb |
5,8
Ac |
6,9
Ab |
9,4
Aa |
7,7
Bb |
|
Pó
de coco |
7,4
ABb |
6,0
Ac |
7,0
Abc |
9,6
Aa |
8,8
Aa |
|
Tropstrato® |
8,0
Ab |
6,0
Ac |
6,6
ABc |
8,7
ABab |
9,0
Aa |
Em
que: Médias seguidas pela mesma letra, maiúscula na coluna e minúscula na
linha, não diferem entre si pelo teste de Tukey a 5% de probabilidade.
TABELA 3: Comprimento (cm/plântula) da
parte aérea e da raiz primária de plântulas de Tabebuia aurea (Silva
Manso) Benth. & Hook. f. ex. S. Moore, oriundas de sementes submetidas a
diferentes temperaturas e substratos.
TABLE 3: Length (cm/seedling) of the shoot and primary
root of Tabebuia aurea (Silva Manso) Benth. & Hook. f. ex. S. Moore seedlings proceeding from seeds submitted at different temperatures and
substrates.
|
Substratos |
Temperatura (oC) |
|
25 |
30 |
35 |
20-30 |
20-35 |
|
|
Comprimento (cm/plântula) da parte aérea |
|
Papel |
4,0 Abc |
5,2 Aab |
6,2 Aa |
3,3 Ac |
4,3 Abc |
|
Areia |
4,2 Ab |
4,4 Ab |
6,3 Aa |
2,1 BCc |
4,1 ABb |
|
Vermiculita |
3,1 Ab |
3,2 Bb |
5,1 Ba |
1,8 Cb |
3,4 Bb |
|
Pó
de coco |
4,6 Ab |
4,9 Ab |
6,8 Aa |
2,4 BCc |
4,2 Ab |
|
Tropstrato® |
4,0 Abc |
4,5 Aab |
6,1 Aa |
2,7 ABc |
3,7 ABbc |
|
|
Comprimento (cm/plântula) da raiz primária |
|
Papel |
12,1 Abc |
13,7 Aa |
12,4 Aab |
11,6 Abc |
10,9 Ac |
|
Areia |
5,4 Cc |
7,4 Ca |
7,0 Bab |
7,0 Cab |
5,8 Cbc |
|
Vermiculita |
7,4 Bb |
9,4 Ba |
7,0 Bb |
8,1 BCab |
2,6 Dc |
|
Pó
de coco |
7,9 Bb |
9,4 Ba |
7,9 Bb |
7,5 BCb |
7,5 Bb |
|
Tropstrato® |
8,4 Bab |
8,7 Bca |
7,1 Bb |
8,3 Bab |
7,7 Bab |
Em
que: Médias seguidas pela mesma letra, maiúscula na coluna e minúscula na
linha, não diferem entre si pelo teste de Tukey a 5% de probabilidade.
Os substratos pó de coco e Tropstrato®, respectivamente, proporcionaram
as melhores combinações (P<0,05) para a massa seca da parte aérea a 30 e
35ºC (Tabela 4). Resultados semelhantes foram obtidos em areia a 30ºC e nos
substratos areia e pó de coco a 35ºC. Comparando-se as temperaturas no
substrato papel, apenas aquelas mais elevadas (30 e 35ºC) mostraram-se
superiores às demais na obtenção de maior acúmulo de massa.
As melhores combinações (P<0,05) para a massa seca do sistema
radicular foram obtidas com o substrato areia a 30 e a 20-30ºC. O papel a 30ºC,
a vermiculita a 30 e 20-30ºC, o pó de coco a 30ºC e o Trospstrato®
a 20-30ºC proporcionaram resultados superiores que nas demais temperaturas
(Tabela 4). Esse teste pode ser usado para se avaliar o crescimento da plântula
e determinar, com maior precisão, a transferência de matéria seca dos tecidos
de reserva para o eixo embrionário na fase de germinação, originando plântulas
com maior peso, em função do maior acúmulo de massa seca (NAKAGAWA, 1999).
No substrato papel foi observado maior comprimento da raiz, no entanto
essas raízes apresentaram-se muito delgadas e com pouquíssimas raízes
secundárias e, portanto, com menor massa seca (Tabelas 3 e 4).
TABELA 4: Massa seca (mg/plântula) da parte aérea e do sistema
radicular de plântulas de Tabebuia aurea (Silva Manso) Benth. &
Hook. f. ex. S. Moore, oriundas de sementes submetidas a diferentes
temperaturas e substratos
TABLE
4:Dry weight matter (mg/seedling) of the aerial part and root system of
Tabebuia aurea (Silva Manso) Benth. & Hook. f. ex. S. Moore
seedlings proceeding from seeds submitted at different temperatures and
substrates.
|
Substratos |
Temperatura (oC) |
|
25 |
30 |
35 |
20-30 |
20-35 |
|
|
Massa seca (mg/plântula) da parte aérea |
|
Papel |
10,5 ABb |
15,4 Ca |
13,2 Ba |
9,2 Ab |
9,8 Bb |
|
Areia |
12,0 Ac |
23,4 ABa |
19,7 Ab |
7,1 ABd |
12,2 ABc |
|
Vermiculita |
8,7 Bc |
13,8 Ca |
11,8 Bab |
5,8 Bd |
10,7 ABbc |
|
Pó de coco |
12,2 Ac |
24,5 Aa |
21,0 Ab |
7,0 ABd |
12,3 Ac |
|
Tropstrato® |
9,8 ABbc |
21,0 Ba |
19,9 Aa |
8,1 ABc |
11,2 ABb |
|
|
Massa
seca (mg/plântula) do sistema radicular |
|
Papel |
10,3 Abb |
13,1 Ba |
11,7 Aab |
11,0 BCb |
11,4 ABab |
|
Areia |
10,9 Ab |
15,4 Aa |
12,2 Ab |
17,4 Aa |
12,7 Ab |
|
Vermiculita |
10,0 Bb |
13,1 Ba |
7,5 Cc |
13,0 Ba |
7,7 Cc |
|
Pó
de coco |
8,8 Cb |
11,7 Ca |
8,7 Bb |
10,3 Cab |
10,8 ABab |
|
Tropstrato® |
7,5 Dbc |
9,7 Dab |
6,9 Cc |
9,9 Ca |
9,2 BCab |
Em
que: Médias seguidas pela mesma letra, maiúscula na coluna e minúscula na
linha, não diferem entre si pelo teste de Tukey a 5% de probabilidade.
A vermiculita não proporcionou resultados satisfatórios, pois, apesar
de apresentar boa capacidade de absorção de água, a umidade era perdida com
maior rapidez, tornando necessário o reumedecimento freqüente desse substrato,
sobretudo em temperaturas mais elevadas. Resultados semelhantes foram obtidos
por Bezerra et al., (2002) com sementes de Momordica charantia
L. em que a vermiculita ocasionou redução na porcentagem e a velocidade de
germinação.
O pó de coco e o Tropstrato® proporcionaram boas combinações para o
comprimento e massa seca da parte aérea. As demais características podem ter
sido comprometidas pelo fato de, mesmo com a capacidade de campo de 60%, a
superfície destes substratos apresentou-se densa em conseqüência da umidade, o
que dificultou a emergência dos cotilédones, reduzindo a velocidade e ampliando
o tempo médio de germinação.
CONCLUSÃO
Os substratos papel toalha e areia favorecema germinação das sementes e o desenvolvimento inicial
das plântulas de Tabebuia aurea sob as temperaturas de 30 e 35ºC.
REFERÊNCIAS
BIBLIOGRÁFICAS
- ANDRADE,
A. C. S.; LOUREIRO, M. B.; SOUZA, A. D. O.; RAMOS, F. N.; CRUZ, A. P. M.
Reavaliação do efeito do substrato e da temperatura na germinação de sementes
de palmiteiro (Euterpe edulis Mart.). Revista Árvore, Viçosa, v.
23, n. 3, p. 279-283, 1999.
- BARBOSA, J. G.; ALVARENGA, E. M.; DIAS, D.
C. F. S.; VIEIRA, A. N. Efeito da escarificação ácida e de diferentes
temperaturas na qualidade fisiológica de sementes de Strelitzia reginae. Revista Brasileira de Sementes, Pelotas, v. 27, n. 1, p. 71-77, 2005.
- BARBOSA,
M. D. Efeito do armazenamento na germinação e vigor de sementes de craibeira
– Tabebuia aurea (Manso) Benth. & Hook.2004.
50f. Dissertação (Mestrado em Ciências Florestais) - Universidade Federal Rural de Pernambuco, Recife, 2004.
- BEWLEY, J. D.; BLACK, M. Seeds: physiology of development
and germination. New York: Plenum Press, 1994. 445p.
- BEZERRA, A. M. E.; MOMENTÉ, V. G.; ARAÚJO,
E. C.; FILHO, S. M. Germinação e desenvolvimento de plântulas de melão-de-são-caetano
em diferentes ambientes e substratos. Revista Ciência Agronômica,
Fortaleza, v. 33, n. 1, p. 39-44, 2002.
- BILIA, D. A. C.; BARBEDO, C. J.; MALUF, A. M. Germinação de
diásporos de canela (Ocotea corymbosa (Meissn.) Mez - Lauraceae) em
função da temperatura, do substrato e da dormência. Revista Brasileira de
Sementes, Brasília, v. 20, n. 1, p. 189-194, 1998.
- BORGES, E. E. L.; RENA, A. B. Germinação de sementes. In: AGUIAR, I. B.; PINÃ-RODRIGUES,
F. C. M. e FIGLIOLIA, M. B. Sementes florestais tropicais. Brasília:
ABRATES, 1993. p.83-135.
- BRASIL.
Ministério da Agricultura e Reforma Agrária. Regras para análise de sementes.
Brasília: SNDA/DNDV/CLAV, 1992. 365p.
- CABRAL, E. L.; BARBOSA, D. C. A.;
SIMABUKURO, E. A. Armazenamento e germinação de sementes de Tabebuia aurea (Manso) Benth. & Hook. f.
ex. S. Moore. Acta
Botanica Brasilica,
São Paulo, v. 17, n. 4,
p. 609-617, 2003.
- CARVALHO, N. M.; NAKAGAWA, J. Sementes:
ciência, tecnologia e produção. Jaboticabal: FUNEP, 2000. 588p.
- CARVALHO, P. E. R. Espécies arbóreas
brasileiras. Colombo: EMBRAPA FLORESTAS (Informação Tecnológica), 2003.
1040p.
- FERREIRA, A. G.; CASSOL, B.; ROSA, S. G. T.; SILVEIRA, T. S.;
STIVAL, A. L.; SILVA, A. A. Germinação de sementes de
Asteraceae nativas no Rio Grande do Sul, Brasil. Acta Botanica Brasilica,
São Paulo, v. 15, n. 2, p. 231-242, 2001.
- FIGLIOLIA, M. B.; OLIVEIRA, E. C.; PINÃ-RODRIGUES, F. C. M. Análise de sementes. In: AGUIAR, I. B.; PINÃ-RODRIGUES,
F. C. M.; FIGLIOLIA, M. B. Sementes florestais tropicais. Brasília:
ABRATES, 1993. p.137-174.
- FREITAS, N. P. Análise do efeito da luz na germinação de
sementes de Tibouchina pulchra Cogn. e Tibouchina sellowiana
Cogn. (Melastomataceae).
1998. 88f. Tese (Doutorado em Ciências Biológicas) - Universidade Estadual Paulista, Rio Claro, 1998.
- GODOI, S.; TAKAKI, M. Effects of light and temperature on seed
germinatin in Cecropia hololeuca Miq. (Cecropiaceae). Brazilian
Archives of Biology and Technology, Curitiba, v.47, n.2, p.185-191, 2004.
- ISTA (INTERNATIONAL SEED TESTING ASSOCIATION). Handbook of
vigour test methods. Zurich: ISTA, 1995. 117p.
- LOPES, J. C.; PEREIRA, M. D.;
MARTINS-FILHO, S. Germinação de sementes de calabura (Mutingia calabura L.). Revista Brasileira de Sementes, Brasília, v. 24, n. 1, p. 59-66,
2002.
- LORENZI, H. Árvores brasileiras: manual de identificação e
cultivo de plantas arbóreas nativas do Brasil. 2.ed. Nova Odessa: Editora
Plantarum, 1998. 352p.
- MACHADO, C. F.; OLIVEIRA, J. A.; DAVIDE, A.C.; GUIMARÃES, R.M. Metodologia
para a condução do teste de germinação em sementes de ipê-amarelo (Tabebuia
serratifolia (Vahl) Nicholson). Cerne, Lavras, v.8, n.2,
p.17-25, 2002.
- MAGUIRE,
J. D. Speed of germination-aid in selection and evaluation for seedlings
emergence and vigor. Crop Science,
Madison, v. 2, n. 1, p. 176-177, 1962.
- MARCOS FILHO, J. Testes de vigor: importância e utilização. In:
KRZYZANOWSKI, F. C.; VIEIRA, R. D.; FRANÇA NETO, J. B. (Eds.) Vigor de
sementes: conceitos e testes. Londrina: ABRATES, 1999. p. 1.1-1.21.
- MARCOS FILHO, J. Fisiologia de sementes de plantas cultivadas. Piracicaba:
Fealq: 2005.495p.
- NAKAGAWA, J. Testes de vigor baseados no desempenho das plântulas.
In: KRZYZANOWSKI, F. C.; VIEIRA, R. D.; FRANÇA NETO, J. B. (Eds.) Vigor de
sementes: conceitos e testes. Londrina: ABRATES, 1999. p. 2.1-2.24.
- POPINIGIS, F. Fisiologia da semente.
5. ed. Brasília: AGIPLAN, 1985. 289p.
- RAMOS, M. B. P.; VARELA, V. P.; MELO, M.
F. F. Influência da temperatura e da água sobre a germinação de sementes de
paricá (Schizolobium amazonicum Huber ex Ducke –
Leguminosae-Caesalpinioidae). Revista Brasileira de Sementes, Brasília, v.28, n.1, p.163-168, 2006.
- ROBERT, R.J. The role of temperature in germination ecophysiology.
In: FENNER, M. Seeds: the ecology of regeneration in plants communities.
Wallingford: CABI, 1992. p.285-325.
- ROSA, S. G. T.; FERREIRA, A. G. Germinação
de sementes de plantas medicinais lenhosas. Acta Botânica Brasilica, São
Paulo, v.15, n.2, p.147-154, 2001.
- SANTOS, D. L.; SUGAHARA, V. Y.; TAKAKI, M.
Efeitos da luz e da temperatura na germinação de sementes de Tabebuia
serratifolia (Vahl) Nich., Tabebuia chrysotricha (Mart ex DC.)
Standl. e Tabebuia roseo-alba (Ridl) Sand – Bignoniaceae. Ciência
Florestal, Santa Maria, v.15, n.1, p.87-92, 2005.
- SILVA, J. B.; NAKAGAWA, J. Estudos de fórmulas para cálculo de
velocidade de germinação. Informativo ABRATES, Brasília, v. 5, n. 1, p.
62-73, 1995.
- SILVA, L. M. M.; RODRIGUES, T. J. D.; AGUIAR, I. B. Efeito da luz
e da temperatura na germinação de sementes de aroeira (Myracrodruon
urundeuva Allemão). Revista Árvore, Viçosa, v.26, n.6, p.691-697,
2002.
- TONETTI, O. A. O.; DAVIDE, A. C.; SILVA,
E. A. A. Qualidade física e fisiológica de sementes de Eremanthus erythropappus (Dc.) Mac. Leish. Revista Brasileira de Sementes, Brasília, v.28, n.1,
p.114-121, 2006.
- TOWNSEND, C. E.; MACGINNIES, W. J. Mechanical
scarification of cicer milkvetch (Astragalus cicer L.). Seed and Crop
Science, Madison, v.12, n.1, p.392-394, 1972.
Copyright 2008 - Ciência Florestal
|
